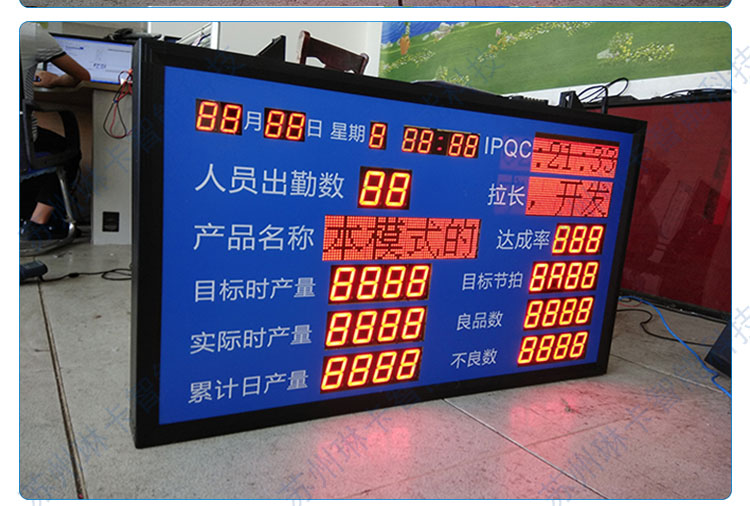
在工業4.0與智能制造浪潮的推動下,車間電子看板系統已成為現代工廠實現精益生產、可視化管理的核心工具。它通過實時顯示生產計劃、進度、質量、設備狀態等關鍵信息,有效提升車間透明度與管理效率。對于有意引入該系統的企業而言,價格、廠家選擇與軟件開發是三大核心關切點。本文將為您提供一站式解析。
一、 車間電子看板系統的價格構成
車間電子看板系統的價格并非單一數字,而是一個由多種因素構成的區間,主要取決于以下要素:
- 硬件成本:包括顯示終端(如LED屏、液晶電視、平板電腦)、工控機、網絡設備、傳感器等。屏幕尺寸、分辨率、安裝方式(壁掛、吊裝)及數量對價格影響顯著。
- 軟件授權費用:這是系統的“大腦”。費用通常基于功能模塊(如生產管理、物料管理、質量管理、設備管理)、用戶數或顯示終端數量來授權。基礎功能版與全功能定制版價格差異巨大。
- 軟件開發與定制費用:如果標準產品無法滿足需求,需要根據企業特定的生產流程、數據接口(與MES/ERP系統對接)、報表格式進行定制開發,這部分是主要的彈性成本。
- 實施與集成服務費:包含現場勘察、系統部署、網絡布線、數據初始化、人員培訓等。項目復雜度越高,服務費占比越大。
- 維護與升級費用:通常以年服務費形式存在,保障系統穩定運行及后續功能升級。
價格區間參考:一套基礎的車間電子看板系統(含少量屏幕及標準軟件)可能從數萬元起步;而大型工廠的全車間、多模塊、深度定制的系統,總投入可達數十萬甚至上百萬元。建議企業明確自身需求,獲取針對性報價。
二、 如何選擇廠家與供應商
選擇可靠的廠家是項目成功的關鍵。除了在“搜了網”等B2B平臺搜索外,還應關注:
- 行業經驗與案例:優先選擇在您所在行業(如汽車零部件、電子裝配、機械加工)有成功案例的廠家。實地考察或參考案例視頻,了解其系統實際運行效果。
- 技術實力與產品成熟度:考察其軟件是否平臺化、可配置,硬件是否穩定可靠。詢問其系統架構、擴展性及與主流工業系統的對接能力。
- 服務能力:本地化或能提供及時響應的技術服務團隊至關重要,這關系到實施效率和后期維護。
- 綜合性價比:并非價格最低就是最好,需綜合評估方案是否符合需求、技術是否先進、服務是否完善。
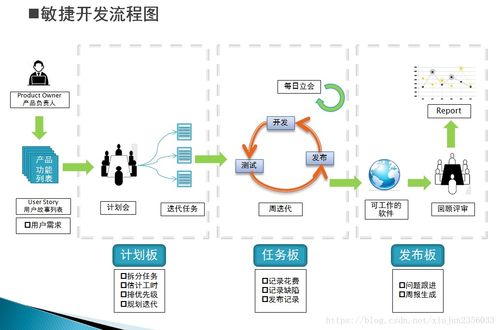
三、 軟件開發:核心中的核心
軟件是電子看板系統的靈魂,其開發應緊扣業務需求:
- 需求分析:與供應商深入溝通,明確需要展示的數據(如生產計劃達成率、生產線實時狀態、不良品率、設備OEE)、展示樣式(圖表、數字、指示燈)、刷新頻率及報警規則。
- 關鍵功能模塊:
- 生產管理看板:實時跟蹤工單進度、生產節拍、完成數量。
- 物料呼叫看板:實現物料短缺時自動呼叫,提升配送效率。
- 質量管理看板:實時監控不良品數量、類型及發生率,定位質量瓶頸。
- 設備管理看板:顯示設備運行、停機、故障狀態,助力預防性維護。
- 安燈系統(Andon):出現異常時快速觸發報警,通知相關人員處理。
- 系統集成:優秀的看板系統必須能與企業現有的MES(制造執行系統)、ERP(企業資源計劃)、WMS(倉儲管理系統)及自動化設備進行數據交互,避免信息孤島。
- 定制化開發:根據車間布局、管理文化進行UI/UX設計,確保信息直觀易懂,真正賦能一線員工與管理者。
四、 實施建議
- 總體規劃,分步實施:可從一條重點產線或一個車間試點,驗證效果后再逐步推廣。
- 數據是基礎:確保數據采集的準確性與實時性,否則看板將失去意義。
- 人員培訓與文化導入:讓員工理解看板的價值,學會利用數據解決問題,而不僅是“被監控”。
****:選購車間電子看板系統是一項系統工程。企業應清晰界定自身需求,在“搜了網”等平臺初選供應商后,進行深入的技術交流與方案評估,重點關注軟件與業務的匹配度及廠家的持續服務能力,從而投資于一套真正能驅動生產效率提升、支撐精益管理的可視化工具。